 人教版九年级化学下册《第九单元 课题3溶液的浓度》导学案(无答案)
人教版九年级化学下册《第九单元 课题3溶液的浓度》导学案(无答案)


《人教版九年级化学下册《第九单元 课题3溶液的浓度》导学案(无答案)》由会员分享,可在线阅读,更多相关《人教版九年级化学下册《第九单元 课题3溶液的浓度》导学案(无答案)(6页珍藏版)》请在装配图网上搜索。
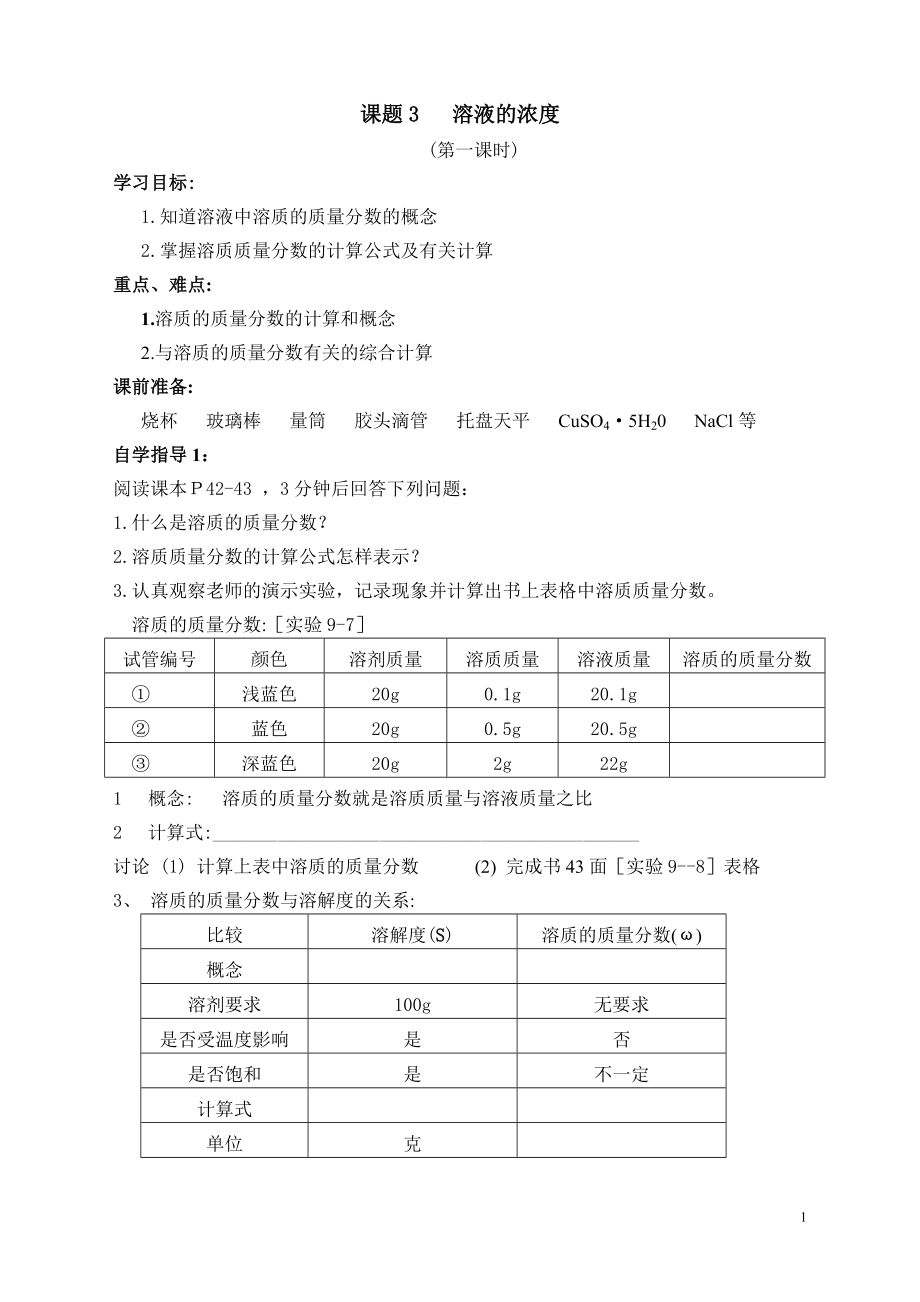
1、课题3 溶液的浓度 (第一课时) 学习目标: 1.知道溶液中溶质的质量分数的概念 2.掌握溶质质量分数的计算公式及有关计算 重点、难点: 1.溶质的质量分数的计算和概念 2.与溶质的质量分数有关的综合计算 课前准备: 烧杯 玻璃棒 量筒 胶头滴管 托盘天平 CuSO45H20 NaCl等 自学指导1: 阅读课本P42-43 ,3分钟后回答下列问题: 1.什么是溶质的质量分数? 2.溶质质量分数的计算公式怎样表示? 3.认真观察老师的演示实验,记录现象并计算出书上表格中溶质质量分数。 溶质的质量分数
2、:[实验9-7] 试管编号 颜色 溶剂质量 溶质质量 溶液质量 溶质的质量分数 ① 浅蓝色 20g 0.1g 20.1g ② 蓝色 20g 0.5g 20.5g ③ 深蓝色 20g 2g 22g 1 概念: 溶质的质量分数就是溶质质量与溶液质量之比 2 计算式:______________________________________________ 讨论 (1) 计算上表中溶质的质量分数 (2) 完成书43面[实验9--8]表格 3、 溶质的质量分数与溶解度的关系: 比较 溶解度(S) 溶质的质量分数(ω)
3、 概念 溶剂要求 100g 无要求 是否受温度影响 是 否 是否饱和 是 不一定 计算式 单位 克 自学指导2: 仔细阅读课本P43的[例题1] ,掌握计算过程 当堂训练: 练习1、20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。 练习2、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。 练习3、配制500mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水各多少克? 堂堂清: 1 常温下,在15克氯化钠中加入60克水,完全溶解后溶液中氯化钠的质量分数为( )
4、 A 15% B 20% C 25% D 33.3% 2 对10%的食盐溶液含义的解释错误的是( ) A 100g食盐溶液中溶解了10g食盐 B 100g水中溶解了10g食盐 C 将10g食盐溶解90g水中所得溶液 D 将食盐和水按1:9的质量比配成所得溶液 3 实验室配制10%的NaCl溶液400g需NaCl______g与 H2O_______g 4 现有100ml的98%的浓硫酸,密度为1.84g/ml,则该硫酸溶液中溶质的质量为多少克? 教学反思:
5、 课题3 溶液的浓度 (第二课时) 学习目标: 1.掌握溶质质量分数的计算要点 2.掌握关于溶质质量分数计算的几种题型 ①溶液的稀释与增浓问题的计算 ②饱和溶液中溶质质量分数的计算 重点、难点: 掌握关于溶质质量分数计算的几种题型 教学过程: 自学指导1: 阅读课本P44 ,3分钟后回答下列问题: 1.有关溶液稀释问题的计算应抓住的关键点是什么? 2.溶液的增浓问题与溶液的稀释有什么联系? 3.饱和溶液中溶质质量分数的计算公式是什么? [题型一] :有关溶液稀
6、释或增浓的计算 计算的依据 : 稀释前溶质质量 = 稀释后溶质质量 增浓前溶质质量 = 增浓后溶质质量 例题1:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液需要多少克水? (课本P44页) 当堂训练1: 练习1:(课本P45)把100g质量分数为98%的浓硫酸 稀释成10%的稀硫酸,需要水的质量是多少? 练习2.有40g溶质质量分数为5%的氯化钠溶液,若将其溶质的质量分数增大到10%,可以采取的方法是? 练习3:将100克10%NaCl溶液转化为20%,求: ① 需要加多少
7、克NaCl? ② 需要蒸发掉多少克水? ③ 需要加40%的NaCl溶液多少克? [题型二]:饱和溶液中溶质质量分数的计算 例2、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。 当堂训练2: 练习1:100C时,NaCl的溶解度是36克。现有50克水放入20克NaCl,求:所得溶液的溶质质量分数 练习2:(课本P45)在20℃时,将40g硝酸钾固体加入100g水中,充分搅拌后,仍有8.4g硝酸钾固体未溶解。请填写下列空白: ① 所得溶液是20℃时硝酸钾的 溶液;(填“饱和”或“不饱”)
8、 ② 20℃时硝酸钾的溶解度为 ; ③ 所得溶液中硝酸钾的质量分数为 。 堂堂清: 1.用25%的NaOH溶液与5%NaOH溶液混合,配制10%的 NaOH溶液,则混合时两溶液的质量之比为多少? 2.已知KNO320℃时的溶解度为31.6克,在该温度下将10克KNO3放入20克水中充分搅拌,所得溶液中溶质的质量分数为多少? 3.实验室要配制50克20%的KNO3溶液,现有25克40%的溶液、20克15%的KNO3溶液、足够多的KNO3晶体和蒸馏水,请用上述物质,设计三种配制方案填入下表: 配制方案
9、(说明配制所需的物质及用量即可) 方案一 方案二 方案三 教学反思: 课题3 溶液的浓度 (第三课时) 学习目标: 1.掌握溶质质量分数在化学方程式计算中的应用。 2.掌握与溶质的质量分数有关的综合计算。 重点、难点: 掌握溶质质量分数在化学方程式计算中的应用。 教学过程: 自学指导: 例题:100g 9.8%硫酸跟多少克锌反应?同时生成多少克氢气? 例题:100g 9
10、.8%硫酸跟多少克锌反应?同时生成多少克氢气? 解:100g9.8%硫酸中含纯硫酸的质量为: 100gx9.8%=9.8g 设参加反应的锌质量为X ,生成氢气的质量为Y Zn + H2SO4 = ZnSO4 + H2 65 98 2 X 9.8g Y X=6.5g Y=0.2g 答:略 当堂训练1: 课本P45:100g某硫酸溶液恰好与13g锌完全反应,试计算这种硫酸中溶质的质量分数。 练习2(课本P45)73g质量分数为20%的盐酸与足量大理石反应,
11、生成二氧化碳的质量是多少?这些二氧化碳的体积(标准状况)是多少?(在标准状况下,CO2的密度为1.977g/L) 练习3、6.5g锌和100g一定质量分数的稀硫酸恰好完全反应,求:(1)生成氢气的质量?(2)稀硫酸中溶质的质量分数?(3)生成的硫酸锌溶液中溶质的质量分数? 练习4 40g10%NaOH溶液跟多少克10%盐酸完全反应?反应后溶液的溶质的质量分数是多少? 练习5. 26g黄铜(Cu-Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为125.8克。求:⑴黄铜中铜的质量分数;⑵反应后所得溶液中溶质质量分数。
12、 练习6 ①将8克SO3溶于92克水中,求所得溶液的溶质的质量分数为多少? ②将250克CuSO45H2O溶于550克水中,溶质的质量分数为多少? 堂堂清: 1. 将10克的KNO3、CaO、Na2CO310H2O分别加到100克的水中溶解,形成的溶液的溶质质量分数最小的是( ) A.KNO3 B.CaO C.Na2CO310H2O D.无法判断 2. 120克稀硫酸与13克锌恰好完全反应。求: ①稀硫酸中溶质的质量分数为多少? ②生成的ZnSO4溶液中溶质的质量分数为多少? 3.含80%的大理石50g加到146稀HCl中(杂质不反应且不溶于水)恰好完全反应。求: ①稀HCl中溶质的质量分数为多少? ②生成的CaCl2溶液中溶质的质量分数为多少? 教学反思: 6
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 36个关键词详解2025政府工作报告
- 学习2025年政府工作报告中的八大科技关键词
- 2025年政府工作报告要点速览接续奋斗共谱新篇
- 学习2025政府工作报告里的加减乘除
- 深化农村改革党课ppt课件(20250305)
- 弘扬雷锋精神凝聚奋进力量学习雷锋精神的丰富内涵和时代价值
- 深化农村改革推进乡村全面振兴心得体会范文(三篇)
- 2025年民营企业座谈会深度解读PPT课件
- 领导干部2024年述职述廉述责述学述法个人报告范文(四篇)
- 读懂2025中央一号党课ppt课件
- 2025年道路运输企业主要负责人安全考试练习题[含答案]
- 2024四川省雅安市中考英语真题[含答案]
- 2024湖南省中考英语真题[含答案]
- 2024宁夏中考英语真题[含答案]
- 2024四川省内江市中考英语真题[含答案]
